Asitler ve Bazlar
Günlük yaşamda sıkça karşılaştığımız, temizlik malzemesi olarak kullandığımız, hatta tükettiğimiz yiyecek ve içeceklerin içerisinde bulunan asitlerin bazların faydalarının yanında zararları da bulunmaktadır. Asit ve bazların oluşturabileceği tehlikeli durumları önlemek için özelliklerinin bilinmesi gerekir.
Asit ve Bazların Genel Özellikleri
Sulu çözeltilerinde Hidrojen (H+) iyonu veren maddeler asit olarak adlandırılır. Genellikle asitlerin formül yapısında hidrojen atomu (H) bulunur. Ancak, yapılarında H bulunmadığı hâlde Karbondioksit (CO2), Azot dioksit (NO2) ve Kükürt dioksit (SO2) maddeleri de asittir.
Benzer şekilde sulu çözeltilerinde Hidroksit (OH–) iyonu veren maddeler baz olarak adlandırılır. Genellikle bazların yapısında hidroksit (OH)– iyonu bulunur. Ancak, OH– bulunmayan amonyak (NH3) da bazdır. NH3 susuz baz olarak da adlandırılır.

Günlük yaşamda asit ve bazlar sulu çözeltilerine verdikleri iyonlarla değil de genel özellikleri sayesinde tanınır. Günlük yaşamda asit ve bazları tanımamıza yarayan genel özellikler aşağıda ele alınmıştır.
Asitlerin Genel Özellikleri
- Asitlerin sulu çözeltilerinin tadı ekşidir. Tükettiğimiz birçok besinin tadının ekşi olmasının nedeni de içerisinde asit bulundurmasıdır. Örneğin tatları genellikle ekşi olan limon, elma, sirke, çilek gibi besinler asit içeren besinlerdir.
- Bazı asitler vücudumuza temas ettiğinde yakıcı ve tahriş edici olabilmektedir. Özellikle, sanayide zaç yağı olarak bilinen ve bazı piller ile araba akülerinde de kullanılan sülfürik asit (H2SO4), temizlik malzemesi olarak kullanılan ve halk arasında tuz ruhu olarak bilinen hidroklorik asit (HCl), halk arasında kezzap olarak bilinen nitrik asit (HNO3) vücutla temas ettiğinde yakıcı ve tahriş edici olabilen kuvvetli asitlere örnektir.
- Asitlerin suda iyonlarına ayrılarak çözündüğünden asitlerin sulu çözeltileri elektrik akımını iletir.
- Asitler, vücuda zarar verebildiği gibi mermer gibi yüzeyleri de aşındırarak zarar verebilmektedir. Bu nedenle özellikle mutfaklarda limon, sirke gibi asit içeren maddeler kullanıldığında tezgâhlarda kullanılan mermerlere zarar verebilmektedir.
- Maddelerin asit içerip içermediğini tespit etmek için turnusol kâğıdı kullanılmaktadır. Asitler mavi turnusol kâğıdının rengini kırmızıya dönüştürürler.
Günlük yaşamda sıkça karşılaşılan asitler aşağıda verilmiştir.
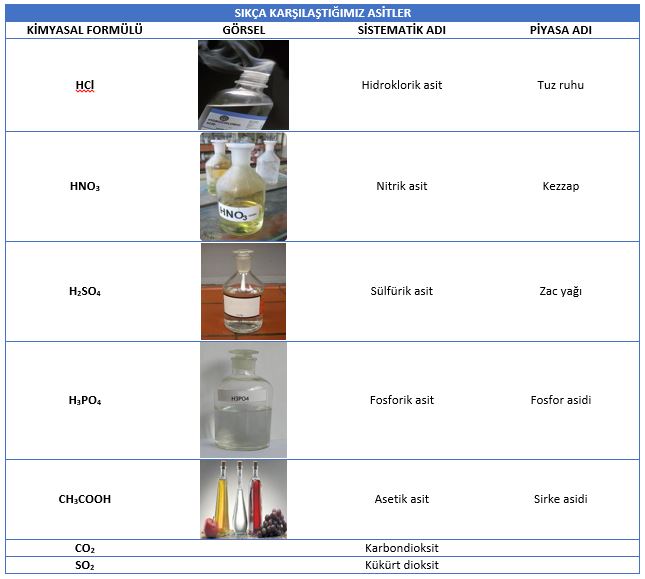
Bazların Genel Özellikleri
- Bazların sulu çözeltilerinin tadı acıdır. Ancak her bazın tadına bakılmaz. Çünkü çok tehlikeli olan bazlar bulunmaktadır.
- Bazlar ele kayganlık hissi verirler. Günlük yaşamda kullandığımız sabun ve şampuan gibi temizlik maddeleri baz içermektedir. Ancak bazların çok tehlikeli olanları başka bir ifadeyle çok kuvvetli olanları da vardır. Bu nedenle kuvvetli bazlar vücutla temas ettiğinde vücudu tahriş ederek tehlikeli sonuçlar doğurabilmektedir.
- Piyasada sud-kostik olarak bilinen ve lavabo açıcı olarak da kullanılan sodyum hidroksit (NaOH), potas-kostik olarak bilinen potasyum hidroksit (KOH), susuz baz olarak bilinen Amonyak(NH3) ve sönmüş kireç olarak bilinen kalsiyum hidroksit (Ca(OH)2) günlük hayatta kullanılan ve sıkça karşılaşılan bazlardandır. Benzer şekilde temizlik malzemesi olarak kullanılan çamaşır suları ve yüzey temizleyiciler de vücuda zarar verebilecek kuvvetli bazları içermektedir.
- Bazlar da asitler gibi suda iyonlarına ayrılarak çözündüğünden elektrik akımını iletir.
- Bazlar kırmızı turnusol kâğıdının rengini maviye dönüştürürler.
Günlük yaşamda sıkça karşılaşılan bazlar aşağıda verilmiştir.
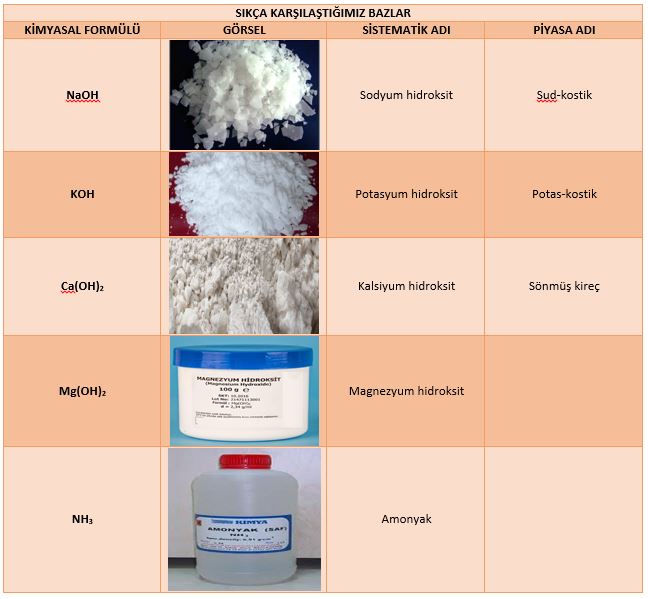
Bir önceki yazımız olan 8. Sınıf Fen Bilimleri Kimyasal Bağ Konu Anlatımı (Yeni Müfredat) başlıklı yazımızda 8.Sınıf Fen Bilimleri Konu Anlatımı, Fen Bilimleri Ders Notları ve Fen Bilimleri Konu Anlatımı hakkında bilgiler verilmektedir.

Guzel ben beğendim ama daha ayrıntılı bilgi verebilir
Zaten genel özellikleri diyor başlıkta